人类将彻底告别骨折损伤,研究人员摸索出骨骼修复新技术
搜狐科技2017/6/1 15:39:28
战争、车祸或是骨密度较低的老年人跌倒造成的骨折,都可能会因损伤程度过于严重而导致骨骼无法完全愈合甚至导致终身残疾。一直以来,人们不断寻找能够治愈骨折的方法。
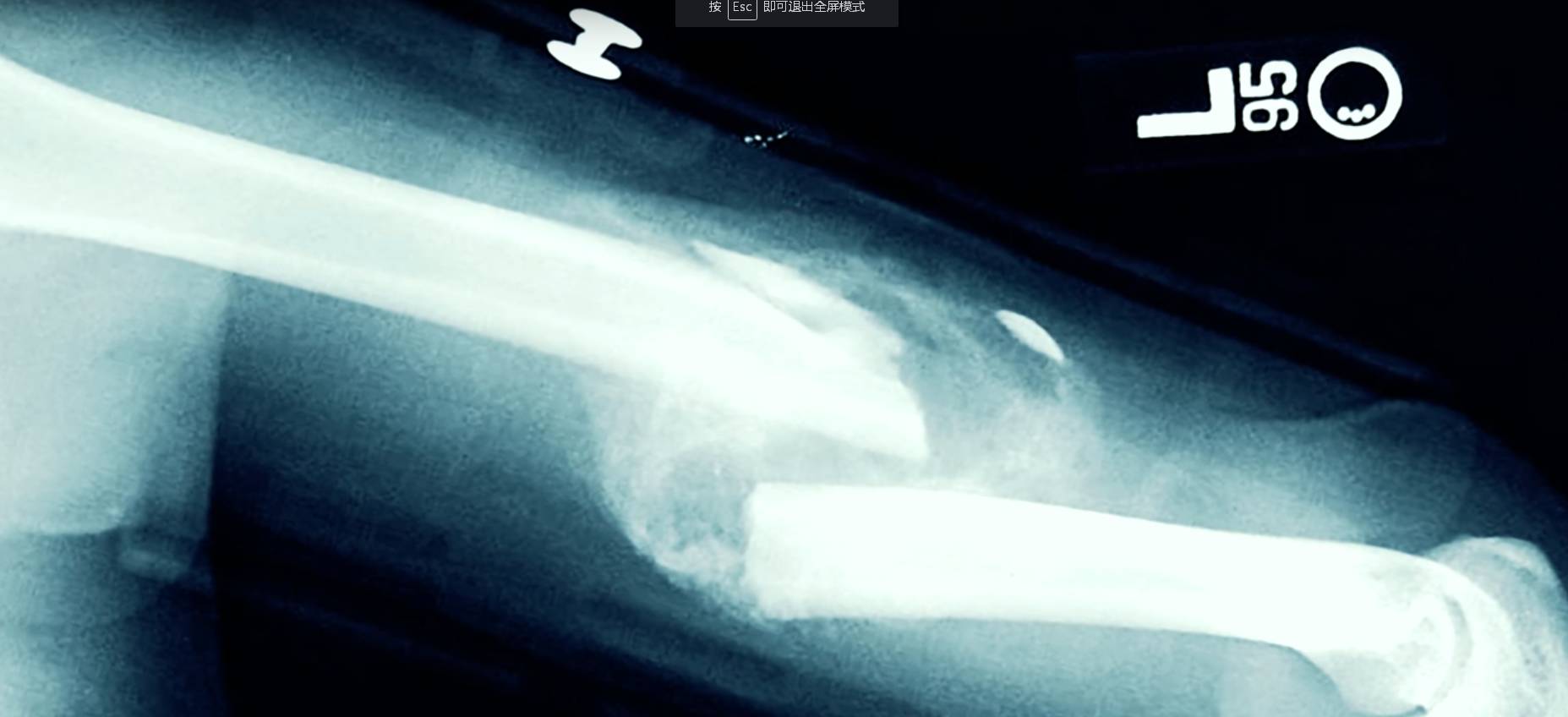
现在,探索终于有了突破,研究人员们结合超声波、干细胞和基因治疗等技术使骨骼损伤得以修复再生。尽管这项技术目前只在动物身上进行过试验,但鉴于其在试验中的完美表现和出色的治愈效果,让这项技术在即将到来的人体临床试验中的表现备受期待。
“ 这项新研究具有重大的临床意义,” 洛杉矶希德斯西奈医学中心整形外科主任David Kulber对其做出很高的评价。“这项能够激活骨骼生长的技术非常值得关注。”

图丨David Kulber医生
同样值得关注的是,每年仅美国就有约10万人因骨骼缺损或骨骼断裂导致的永久性骨损伤而备受折磨。遇到这种情况,医生通常会为患者进行植骨手术,将另一块骨组织移植到骨折的空隙中间。
理想状态下,移植用的骨组织来源于病人自体——常取用髂骨的一部分,而取骨手术又相当于一次严重创伤,往往令患者 “雪上加霜”。因此,骨科医生转向 从尸体中获得用于植骨术的骨骼。然而,从尸体上取骨后的灭菌步骤又破坏了许多促进骨骼生长的关键蛋白及其他信号分子,大大降低了植骨后骨折完全愈合的几 率。
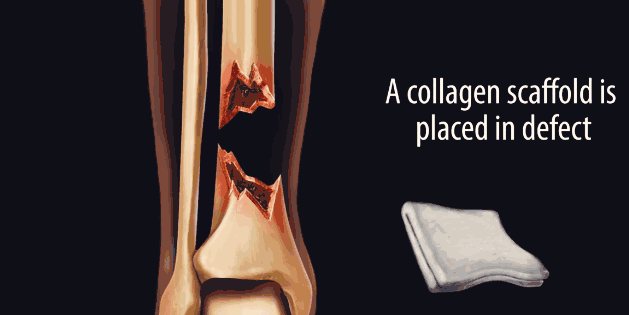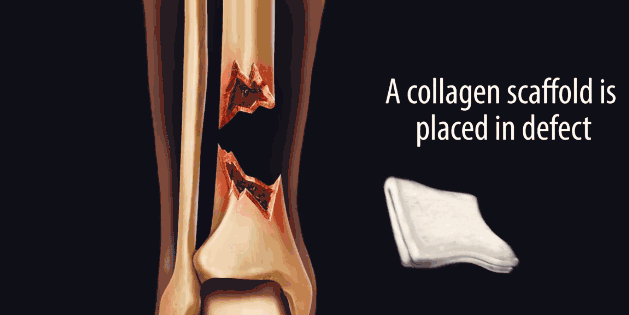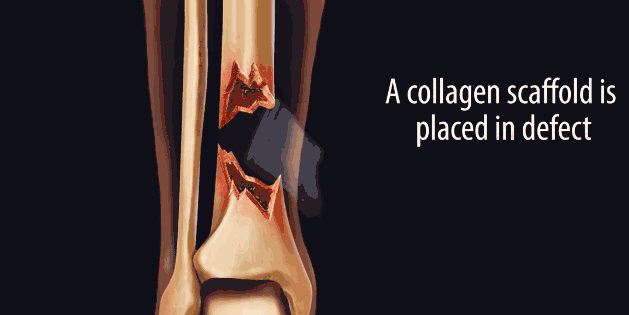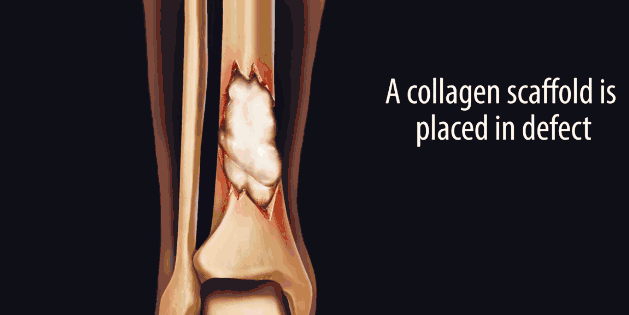
因此,研究人员一直希望能够通过使骨骼再生的方式来代替植骨。他们首先尝试将一种“天然支架”蛋白——胶原蛋白,填充至骨折两端之间的缝隙中。胶原 蛋白将会诱导人体中分化成骨骼的干细胞——间充质干细胞迁移至骨折缝隙间,进行下一步分化。但事实上,间充质干细胞并非特异性分化为骨细胞,它作为一种多 能干细胞,同样可能分化形成脂肪组织或瘢痕组织。
多年以来,研究人员致力于探索将间充质干细胞定向诱导分化为骨细胞的方法。为此他们尝试将间充质干细胞暴露于不同类型的骨形态发生蛋白(bone morphogenetic proteins, BMPs),即一类诱导间充质干细胞分化为骨组织的生长因子。间充质干细胞需要在BMPs中暴露约一周时间才能够完成分化过程,而定点注射至骨折部位的 BMPs却只有几小时的有效时间,一次注射远远无法做到刺激骨组织再生。
为构建出长效作用的BMPs,由希德斯西奈医学中心再生医学专家Dan Gazit率领的研究团队及其他课题组尝试利用病毒将BMP基因导入间充质干细胞中,使其自身持续表达BMPs,并刺激其分化。然而这一尝试并未收获令人满意的结果。

最近几年,Gazit团队研发出了可代替病毒将基因导入间充质干细胞的新策略:首先,他们在骨折处填充满胶原蛋白并等待干细胞迁移浸润;几周后,他 们将大量目标基因片段与由气体填充、脂分子包裹的微型囊泡混合,注射至骨折处;随后,他们还需要在创伤处及周围施加超声波——就像产科医生检查胎儿一样。 超声波能够使注射的微囊泡爆裂,冲击使附近干细胞的胞膜上短暂产生纳米级尺寸的洞,使基因能够顺利进入细胞内。
2014年,Gazit团队报道了他们在动物骨折样本中采取这种方法成功导入了无治疗作用的报告基因。然而当他们用同样方法导入两种不同亚型BMPs——BMP-2和BMP-7基因后,他们发现骨骼的确再生了,但并不够使骨折愈合。
Gazit团队在通过手术将BMP-6基因插入到所构建的1厘米缝隙的腿骨缺损样本中之后,得到了令人欣慰的结果:治疗八周后,他们发现全部的治疗组动物骨缝隙都不复存在,骨折完全愈合。

事实证明,这项当前备受推崇的新治疗方法,与过去自体骨移植有着同样好的治疗效果。这一成果发表在了5月17日的《科学-转化医学》(Science Translational Medicine)上。
“这一研究结果说明我们非常需要继续发展利用干细胞再生骨组织治疗骨折,”德克萨斯大学健康科学中心骨科研究员Johnny Huard说道。“然而,这项研究中使用的猪样本年龄全部不足一年。年轻的动物和人类比老年拥有更多的间充质干细胞,并且老年人骨折的损伤程度往往远大于 年轻人。” 因此,Huard建议在尝试治愈人类骨折之前,仍需要观察此方法用于老年动物骨折样本中是否同样有效。
编辑 田雨
